Chuyên đề 12. Hiđrocacbon
Phản ứng cháy của ankađien
- Chi tiết
- Chuyên mục: Chuyên đề 12. Hidrocacbon
- Được viết ngày Thứ năm, 01 Tháng 1 2015 22:09
- Viết bởi Nguyễn Văn Đàm
Cũng như các hiđrocacbon khác ankađien dễ dàng tham gia phản ứng cháy cho sản phẩm gồm CO2 và H2O theo phương trình tổng quát sau:
CnH2n-2 + (3n-1)/2 O2 → n CO2 + (n-1)H2O
Dựa vào phương trình phản ứng trên ta có thể nhận thấy đặc điểm phản ứng cháy của ankađien:
Phản ứng cộng của ankađien
- Chi tiết
- Chuyên mục: Chuyên đề 12. Hidrocacbon
- Được viết ngày Thứ ba, 30 Tháng 12 2014 10:32
- Viết bởi Nguyễn Văn Đàm
- Ankađien chứa liên kết đôi trong phân tử vì vậy phản ứng đặc trưng của ankađien là phản ứng cộng (tương tự như anken).
- Vi chứa 2 liên kết đôi C=C nên ankađien có thể tham gia vào phản ứng cộng theo tỉ lệ mol 1:1 hoặc 1:2. Phức tạp nhất là trường hợp cộng vào ankađien liên hợp.
- Phản ứng cộng của ankađien có thể xảy ra với các tác nhân: H2, dung dịch Br2 và HX và cũng tuân theo các quy tắc như trường hợp cộng vào anken.
- Dưới đây ta chỉ xét phản ứng cộng vào ankađien liên hợp:
Lý thuyết về ankađien
- Chi tiết
- Chuyên mục: Chuyên đề 12. Hidrocacbon
- Được viết ngày Thứ ba, 30 Tháng 12 2014 10:18
- Viết bởi Nguyễn Văn Đàm
- Ankađien là những hiđrocacbon không no, mạch hở trong phân tử có chứa 2 liên kết đôi còn lại là các liên kết đơn.
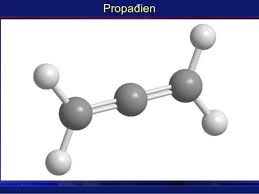
Ankadien đơn giản nhất - C3H4
- Công thức tổng quát: CnH2n-2 (n ≥ 3).
- Danh pháp thay thế: số chỉ vị trí nhánh + tên nhánh + tên mạch chính + a + số chỉ vị trí nối đôi + đien.
Phản ứng cộng của anken
- Chi tiết
- Chuyên mục: Chuyên đề 12. Hidrocacbon
- Được viết ngày Thứ ba, 30 Tháng 12 2014 09:54
- Viết bởi Nguyễn Văn Đàm
Do chứa liên kết pi kém bền (nằm trong liên kết đôi C=C) nên phản ứng đặc trưng của anken là phản ứng cộng với trung tâm phản ứng là liên kết đôi C=C.
1. Cộng H2
CnH2n + H2 → CnH2n+2 (Ni, t0)
Đặc điểm của phản ứng cộng H2 vào anken:
+ Tỉ khối của hỗn hợp khí sau phản ứng bao giờ cũng tăng (do số mol khí giảm còn khối lượng thì không đổi) do đó ntrước.Mtrước = nsau.Msau.
Phản ứng cháy của anken
- Chi tiết
- Chuyên mục: Chuyên đề 12. Hidrocacbon
- Được viết ngày Thứ hai, 29 Tháng 12 2014 10:46
- Viết bởi Nguyễn Văn Đàm
Cũng như ankan, anken tham gia phản cháy dễ dàng cho sản phẩm cháy là H2O và khí CO2. Với cùng số nguyên tử C thì nhiệt lượng giải phóng của anken lớn hơn do sinh ra ít nước hơn.
- Phản ứng cháy tổng quát của anken là:
CnH2n + 3n/2O2 → nCO2 + nH2O
Lý thuyết về anken
- Chi tiết
- Chuyên mục: Chuyên đề 12. Hidrocacbon
- Được viết ngày Thứ hai, 29 Tháng 12 2014 10:30
- Viết bởi Nguyễn Văn Đàm
I. KHÁI NIỆM, ĐỒNG PHÂN, DANH PHÁP
- Anken hay olefin là hiđrocacbon không no, mạch hở trong phân tử có chứa 1 liên kết đôi C=C còn lại là các liên kết đơn.
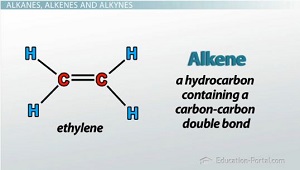
- Công thức tổng quát của anken: CnH2n (n ≥ 2).
- Tên gọi:
+ Tên thay thế:
Số chỉ vị trí mạch nhánh + tên nhánh + tên mạch chính + số chỉ vị trí nối đôi + en
+ Tên thường:
Thay đuôi ‘an’ của ankan bằng đuôi ‘ilen’
Lí thuyết về xicloankan
- Chi tiết
- Chuyên mục: Chuyên đề 12. Hidrocacbon
- Được viết ngày Thứ bảy, 27 Tháng 12 2014 00:37
- Viết bởi Nguyễn Văn Đàm
- Xicloankan là hiđrocacbon no mạch vòng. Thường chỉ xét xicloankan đơn vòng.
- Công thức tổng quát của monoxicloankan: CnH2n (n ≥ 3).
- Tên thay thế:
Số chỉ vị trí mạch nhánh (nếu có nhiều nhánh) + tên nhánh + xiclo + tên mạch chính + an
- Đồng phân của xicloankan có các loại: đồng phân anken; đồng phân về độ lớn của vòng (n ≥ 4), đồng phân vị trí nhánh trên vòng (n ≥ 5), đồng phân về cấu tạo nhánh (n ≥ 6), đồng phần hình học với vòng 3 cạnh.
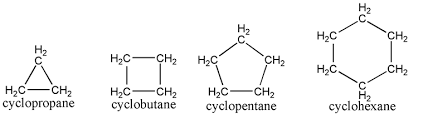
Một số xicloankan đơn giản
Các phản ứng do tác dụng của nhiệt của ankan
- Chi tiết
- Chuyên mục: Chuyên đề 12. Hidrocacbon
- Được viết ngày Thứ sáu, 26 Tháng 12 2014 16:15
- Viết bởi Nguyễn Văn Đàm
Ankan tham gia vào nhiều phản ứng do tác dụng của nhiệt như phản ứng tách hiđro, phản ứng crăcking, phản ứng phân huỷ và phản ứng cháy. Trong nội dung bài này chỉ đề cập đến phản ứng tách hiđro, phản ứng phân huỷ và phản ứng crăcking.
1. Phản ứng tách H2 (phản ứng đề hiđro hóa)
CnH2n+2 → CnH2n + H2 (Fe, t0)
Anken
Chú ý:
Phản ứng thế của ankan
- Chi tiết
- Chuyên mục: Chuyên đề 12. Hidrocacbon
- Được viết ngày Thứ sáu, 26 Tháng 12 2014 15:58
- Viết bởi Nguyễn Văn Đàm
Phản ứng thế là phản ứng đặc trưng của ankan vì phân tử ankan chỉ chứa liên kết đơn.
1. Phản ứng thế (Cl2/as hoặc Br2/t0)
CnH2n+2 + xX2 → CnH2n+2-xXx + xHX
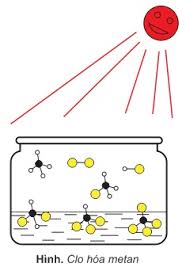
- Về nguyên tắc các nguyên tử H trong phân tử ankan có thể bị thay thế lần lượt từ 1 đến hết.
- Khả năng phản ứng giảm theo thứ tự F2 > Cl2 > Br2 > I2.
Phản ứng cháy của ankan
- Chi tiết
- Chuyên mục: Chuyên đề 12. Hidrocacbon
- Được viết ngày Thứ sáu, 26 Tháng 12 2014 15:31
- Viết bởi Nguyễn Văn Đàm
Các ankan đều rất dễ tham gia phản ứng cháy sinh ra sản phẩm là CO2 và H2O kèm theo sự tỏa nhiệt mạnh. Vì vậy ankan được dùng nhiều làm nhiên liệu như khí ga để đun nấu là metan, để nạp vào bật lửa như propan và butan, để làm xăng dầu như octan, nonan... để làm nến như các ankan rắn.
Phản ứng cháy tổng quát của ankan là
CnH2n+2 + (3n + 1)/2O2 → nCO2 + (n + 1)H2O
Page 3 of 4