Chuyên đề 1. Cấu tạo nguyên tử, bảng tuần hoàn, liên kết hóa học
Độ phân cực của liên kết, hoá trị
- Chi tiết
- Chuyên mục: Chuyên đề 1. Cấu tạo nguyên tử, bảng tuần hoàn, liên kết hóa học
- Được viết ngày Thứ hai, 09 Tháng 2 2015 15:20
- Viết bởi Nguyễn Văn Đàm
I. ĐỘ PHÂN CỰC CỦA LIÊN KẾT HÓA HỌC
Để xác định độ phân cực của liên kết hóa học có thể dựa theo 2 cách:
- Định lượng: dựa vào hiệu độ âm điện của 2 nguyên tử tham gia liên kết. Theo cách này, hiệu độ âm điện càng lớn thì liên kết càng phân cực.

- Định tính: độ phân cực của liên kết tăng dần theo dãy: liên kết cộng hóa trị không phân cực < liên kết cộng hóa trị phân cực < liên kết ion.

Chú ý:
- Chỉ dùng cách định lượng khi bài cung cấp giá trị độ âm điện của các nguyên tố.
- Cần phân biệt sự phân cực của liên kết với sự phân cực của các phân tử:
+ Các hợp chất ion là các phân tử có cực.
+ Các hợp chất cộng hóa trị không phân cực là các phân tử không cực.
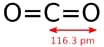
+ Các hợp chất chứa liên kết cộng hóa trị phân cực có thể là phân tử phân cực hoặc không.
II. HÓA TRỊ CỦA NGUYÊN TỐ TRONG CÁC LOẠI HỢP CHẤT
- Trong hợp chất ion, điện hóa trị của 1 nguyên tố bằng điện tích của ion và được gọi là điện hóa trị của nguyên tố đó.
- Trong hợp chất cộng hóa trị, hóa trị của một nguyên tố được xác định bằng số liên kết của nguyên tử nguyên tố đó trong phân tử và được gọi là cộng hóa trị của nguyên tố đó.
Hochoaonline.net giới thiệu đến các bạn các bài tập tham khảo sau: