Bài toán đốt cháy amin
- Chi tiết
- Chuyên mục: Chương 3. Amin, Amino Axit và Protein
- Được viết ngày Thứ hai, 16 Tháng 3 2015 14:49
- Viết bởi Nguyễn Văn Đàm
Amin là hợp chất hữu cơ chứa C, H, N nên khi đốt cháy amin sản phẩm thu được gồm CO2, H2O và N2 theo phương trình tổng quát sau:
CxHyNz + (x+y/4)O2 → xCO2 + y/2H2O + z/2N2
Chúng ta thường gặp với amin no đơn chức mạch hở thì:
CnH2n+3N + (6n+3)/4 O2 → nCO2 + (n+3/2)H2O + 1/2N2
Lý thuyết về amin
- Chi tiết
- Chuyên mục: Chương 3. Amin, Amino Axit và Protein
- Được viết ngày Thứ hai, 16 Tháng 3 2015 14:53
- Viết bởi Nguyễn Văn Đàm
I. ĐỊNH NGHĨA
- Các định nghĩa về amin:
+ Amin là sản phẩm thu được khi thay thế nguyên tử H trong phân tử NH3 bằng các gốc hiđrocacbon. (chỉ đúng với amin đơn chức):
Amoniac
+ Amin là sản phẩm thu được khi thay thế nguyên tử H trong hidrocacbon bằng nhóm -NH2 (chỉ đúng với amin bậc 1).
+ Amin là hợp chất hữu cơ trong phân tử chỉ chứa 3 nguyên tố: C, H và N.
Lý thuyết về aminoaxit
- Chi tiết
- Chuyên mục: Chương 3. Amin, Amino Axit và Protein
- Được viết ngày Thứ hai, 16 Tháng 3 2015 14:57
- Viết bởi Nguyễn Văn Đàm
I. ĐỊNH NGHĨA
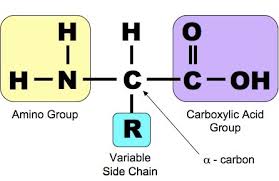
- Aminoaxit là những hợp chất hữu cơ tạp chức trong phân tử có chứa đồng thời 2 nhóm chức: nhóm amino (NH2) và nhóm cacboxyl (COOH).
- Công thức tổng quát của aminoaxit: R(NH2)x(COOH)y hoặc CnH2n+2-2k-x-y(NH2)x(COOH)y.
Quan trọng nhất là các α - aminoaxit (các aminoaxit có các nhóm COOH và NH2 cùng gắn vào 1 nguyên tử C - C số 2). Hầu hết các aminoaxit thiên nhiên đều là các α - aminoaxit.
Lý thuyết về peptit, protein và một số hợp chất hữu cơ chứa nitơ
- Chi tiết
- Chuyên mục: Chương 3. Amin, Amino Axit và Protein
- Được viết ngày Thứ hai, 16 Tháng 3 2015 15:00
- Viết bởi Nguyễn Văn Đàm
A. PEPTIT
I. Khái niệm
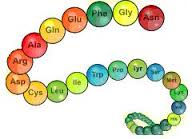
- Liên kết của nhóm CO với nhóm NH giữa hai đơn vị α - aminoaxit được gọi là liên kết peptit.
- Peptit là những hợp chất chứa từ 2 đến 50 gốc α - aminoaxit liên kết với nhau bằng các liên kết peptit.
II. Phân loại
Một số phản ứng khác của aminoaxit
- Chi tiết
- Chuyên mục: Chương 3. Amin, Amino Axit và Protein
- Được viết ngày Thứ hai, 16 Tháng 3 2015 15:02
- Viết bởi Nguyễn Văn Đàm
Ngoài các phản ứng đặc trưng hay gặp của aminoaxit thể hiện tính lưỡng tính, aminoaxit còn có một số phản ứng khác như:
- Phản ứng cháy
- Phản ứng este hóa
- Phản ứng trùng ngưng
Muối và este của aminoaxit
- Chi tiết
- Chuyên mục: Chương 3. Amin, Amino Axit và Protein
- Được viết ngày Thứ hai, 16 Tháng 3 2015 15:04
- Viết bởi Nguyễn Văn Đàm
A. MUỐI CỦA AMINOAXIT
Có hai loại muối của aminoaxit thường gặp là muối của aminoaxit với axit vô cơ dạng ClNH3-R-COOH và NH2-R-COONa trong đó ClNH3-R-COOH có tính axit còn NH2-R-COONa có tính bazơ. Ngoài ra hiếm gặp hơn là muối dạng R-COONH3-R'-COOH có tính lưỡng tính.
Muối và este của aminoaxit
- Chi tiết
- Chuyên mục: Chương 3. Amin, Amino Axit và Protein
- Được viết ngày Thứ hai, 16 Tháng 3 2015 15:06
- Viết bởi Nguyễn Văn Đàm
A. MUỐI CỦA AMINOAXIT
Có hai loại muối của aminoaxit thường gặp là muối của aminoaxit với axit vô cơ dạng ClNH3-R-COOH và NH2-R-COONa trong đó ClNH3-R-COOH có tính axit còn NH2-R-COONa có tính bazơ. Ngoài ra hiếm gặp hơn là muối dạng R-COONH3-R'-COOH có tính lưỡng tính.
Phản ứng của amin với dung dịch Brom và axit Nitrơ
- Chi tiết
- Chuyên mục: Chương 3. Amin, Amino Axit và Protein
- Được viết ngày Thứ hai, 16 Tháng 3 2015 15:09
- Viết bởi Nguyễn Văn Đàm
A. PHẢN ỨNG VỚI HNO2
Để phân biệt amin các bậc với nhau thì ngoài phản ứng với thuốc thử Lucas, trong chương trình hóa học phổ thông chúng ta thường sử dụng axit nitro HNO2.
- Amin bậc 1 tác dụng với HNO2 tạo thành ancol, N2 và nước tương tự amoniac:
R - NH2 + HNO2 → ROH + N2 + H2O
Phản ứng thủy phân peptit và protein
- Chi tiết
- Chuyên mục: Chương 3. Amin, Amino Axit và Protein
- Được viết ngày Thứ hai, 16 Tháng 3 2015 15:11
- Viết bởi Nguyễn Văn Đàm
Peptit là hợp chất hữu cơ gồm 2 đến 50 gốc α - aminoaxit liên kết với nhau bằng liên kết peptit. (Liên kết peptit là liên kết -CO-NH- giữa các α - aminoaxit). Các bạn chú ý phân biệt nhóm peptit và nhóm amit nhé.
Peptit và protein có hai dạng thủy phân là thủy phân hoàn toàn và thủy phân không hoàn toàn.
Tính bazơ của amin
- Chi tiết
- Chuyên mục: Chương 3. Amin, Amino Axit và Protein
- Được viết ngày Thứ hai, 16 Tháng 3 2015 15:13
- Viết bởi Nguyễn Văn Đàm
Amin là dẫn xuất của amoniac vì vậy tính chất của amin có nhiều điểm tương tự amoniac. Cũng như amoniac tính bazơ của amin là do nguyên tử N trong amin còn một cặp electron chưa tham gia liên kết có khả năng nhận proton (H+). Điện tích âm ở nguyên tử N càng lớn khả năng nhận H+ càng tăng thì tính bazơ càng mạnh. Khi nguyên tử N liên kết với các gốc hiđrocacbon no (tác nhân đẩy e) thì làm tăng tính bazơ, còn nếu nguyên tử N liên kết với gốc hiđrocacbon không no, thơm (tác nhân hút e) thì tính bazơ giảm. Tóm lại thứ tự tính bazơ được xếp theo chiều tăng dần là: